Contenidos
- Cancer sintomas .com
- Cáncer de piel
- Cáncer de tiroides
- Cáncer de colon
- Cáncer de mama
- Cáncer de garganta (laringe)
- Cáncer de estómago
- Cáncer de vagina (vaginal)
- Cáncer oral (de boca)
- Cáncer de próstata
- Cáncer de huesos (óseo)
- Cáncer de vulva (vulvar)
- Cáncer de pulmón
- Cáncer de útero
- Cáncer de vejiga
- Cáncer de hígado
- Cáncer de ano (anal)
- Cáncer de pene
- Leucemia (cáncer en la sangre)
- Tumor cerebral (cáncer de cerebro)
- Cáncer de páncreas
- Cáncer rectal
- Mieloma múltiple
- Cáncer de riñón
- Cáncer de vesícula biliar
- Cáncer de glándulas salivales
- Cáncer de cuello uterino (cervical)
- Cáncer de ovario
- Cáncer de ojo (ocular)
- Cáncer de esófago (esofágico)
- Cáncer de corazón
- Cáncer de testículo
- Linfoma (de Hodgkin y no)
- Retinoblastoma
- Tumor de Wilms
- Neuroblastoma
- Mesotelioma
- Rabdomiosarcoma
- Imágenes contra el cáncer
- Asociación Americana del Cáncer (Sociedad ACS)
Versão em português
También de interés
Publicidad
Síntomas de leucemia
Primeros signos comunes de tumor sanguíneo, información sobre las señales iniciales de carcinoma y neoplasia sanguínea fulminante, en adultos y niños (infantil), y en hombres y mujeres.
Los síntomas de leucemia (un tipo de cáncer de la sangre) comienzan a aparecer cuando el número de células cancerígenas (anormales) en la sangre crece y la médula ósea no puede fabricar las células normales de la sangre que el cuerpo necesita. La leucemia consiste en una sobreproducción de células anormales o que se "atascan" en una fase temprana del proceso de maduración. Estas células leucémicas no son funcionales y no son capaces de hacer el trabajo de las células sanguíneas maduras sanas.
Tener pocas células normales en la sangre, sean glóbulos blancos, glóbulos rojos, o plaquetas, puede causar una serie de síntomas. En la leucemia aguda, los síntomas aparecen y empeoran rápidamente.
Los signos y síntomas de la leucemia son: fatiga, malestar, pérdida de apetito, pérdida de peso, fiebre, anemia, falta de aliento, palidez, palpitaciones (latidos rápidos del corazón), debilidad, mareo, moratones generalizados, hemorragias nasales frecuentes o graves, sangrado de las encías, flujo menstrual abundante, puntos rojos en la piel (petequias), infecciones frecuentes (neumonía, cistitis, infección de encías o alrededor del ano, herpes labial), vómitos, dolor de cabeza, dolor de garganta, sudores nocturnos, dolor en los huesos y las articulaciones, ganglios linfáticos agrandados (en el cuello, las axilas, la ingle o encima de la clavícula), malestar abdominal o sensación de estar lleno, problemas de la vista, llagas en los ojos e hinchazón de los testículos.
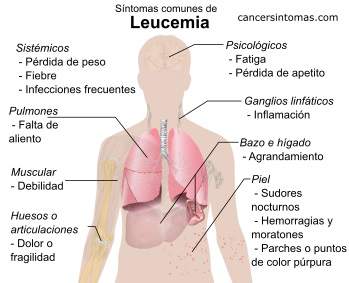 |
- Cloroma (sarcoma granulocítico), un grupo de células de leucemia bajo la piel o en otras partes del cuerpo, similar a un tumor.
- Cambios en la piel:
* Leucemia de cutis: ocurre cuando las células de la leucemia entran en la piel. Las llagas o parches pueden ser de cualquier tamaño y suelen ser de color rosa o canela.
* Vasculitis leucocitoclástica: se asemeja a una reacción alérgica en la piel. Las úlceras suelen aparecer en las extremidades (manos y pies).
* Síndrome de Sweet (dermatosis neutrofílica febril aguda): con fiebre y llagas dolorosas que pueden aparecer en cualquier parte del cuerpo.
Leucemia aguda
Otros síntomas de la leucemia aguda pueden incluir: fiebre, escalofríos, pérdida de peso inexplicable, infecciones frecuentes, dolor o sensación de plenitud debajo de las costillas, malestar general, dolor de garganta, inflamación de las encías, sudoración nocturna, dolor de cabeza, vómitos, problemas de visión, dolor de huesos o articulaciones (sobre todo en la cadera o el esternón), e hinchazón indolora de los ganglios linfáticos.
Cuando se diagnostica la leucemia aguda, por lo general hay ya un número grande y creciente de células leucémicas. Los signos y síntomas pueden haber estado presentes menos de tres meses, o incluso tan sólo unos días.
Entre los tipos de leucemia aguda están la leucemia linfocítica aguda y la leucemia mieloide aguda.
Leucemia crónica
En las etapas iniciales de la leucemia crónica, las células leucémicas pueden funcionar casi normalmente y no causan síntomas. La enfermedad a menudo se descubre durante un análisis de sangre rutinario. Cuando los síntomas aparecen, por lo general son leves al principio y empeoran gradualmente. Los síntomas de la leucemia crónica pueden incluir: fatiga persistente, debilidad, malestar general, pérdida de apetito, pérdida de peso inexplicable, sudoración excesiva (sobre todo de noche), inflamación sin dolor de los ganglios linfáticos, y agrandamiento del hígado o el bazo.
Las personas con leucemia aguda son más propensas a experimentar los primeros síntomas de la enfermedad que aquellas personas con las formas crónicas de este cáncer. En muchos casos, las personas con leucemia crónica no tienen síntomas iniciales, por lo que suele ser frecuente que se descubra la enfermedad en un chequeo rutinario.
Con frecuencia, estos síntomas no son causados por la leucemia sino que pueden deberse a otros problemas de salud como la gripe o una infección. Se necesitan pruebas para hacer un diagnóstico. Debería acudir al médico si presenta cualquier signo o síntoma de los indicados de una forma persistente.
¿Qué es la leucemia?
La leucemia es un cáncer que comienza en las células madre que forman la sangre en la médula ósea. Por lo general, afecta a las células blancas de la sangre. Sin embargo, otras células de la sangre también pueden estar implicadas.
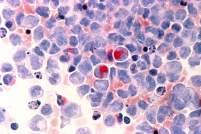 |
La leucemia se desarrolla cuando las células madre de la sangre en la médula ósea cambian en su ADN y ya no crecen o se comportan anormalmente. Estas células anormales se denominan células de leucemia. Con el tiempo, las células leucémicas desplazan a las células normales de la sangre para que no puedan hacer su trabajo.
Tipos de leucemia
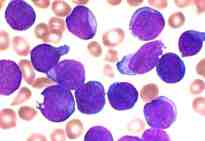 |
En los adultos, la linfocítica crónica y la mielógena aguda son las leucemias más comunes. Existen muchos subtipos diferentes de leucemia.
Leucemia aguda
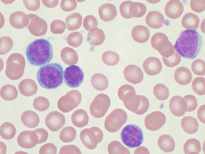 |
Leucemia crónica
En la leucemia crónica, las células de la médula ósea maduran en parte y tienen un aspecto más normal que las células inmaduras de la leucemia aguda. La leucemia crónica por lo general avanza lentamente y permite que las células cancerosas se desarrollen más. Estas células sobreviven más tiempo, por lo que se acumulan y desplazan a las células normales. En general, estas células pueden desempeñar algunas de las funciones normales.
Leucemias linfocíticas raras
Existen varios tipos raros de leucemia linfocítica que comparten algunas características con la leucemia linfocítica crónica:
- la leucemia prolinfocítica;
- la leucemia de grandes linfocitos granulares;
- la leucemia linfocítica de células T grandes y granulares;
- la leucemia agresiva de células NK;
- el linfoma de células T adultas;
- el síndrome de Sézary (fase leucémica del linfoma cutáneo de células T);
- la leucemia de células peludas.
Trastornos relacionados con la leucemia
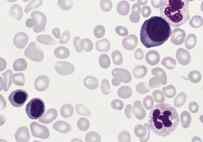 |
Los trastornos mieloproliferativos
En los trastornos mieloproliferativos se produce un exceso de uno o más tipos de células sanguíneas (glóbulos rojos, glóbulos blancos o plaquetas). La sobreproducción se inicia cuando una sola célula madre muta y se reproduce. Hay 4 tipos de trastornos mieloproliferativos: policitemia vera o policitemia vera rubra, mielofibrosis idiopática, trombocitemia esencial o trombocitosis y leucemia mielógena crónica.
Los síndromes mielodisplásicos
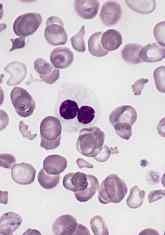 |
Síndromes mielodisplásicos / mieloproliferativos
Los síndromes mielodisplásicos / mieloproliferativos tienen características de ambos síndromes: los mielodisplásicos y los trastornos mieloproliferativos. Entre ellos están:
- la leucemia mielomonocítica crónica;
- la leucemia mielógena crónica atípica;
- el trastorno mielodisplásico / mieloproliferativo inclasificable.
Una vez que el tipo de leucemia o trastorno relacionado ha sido diagnosticado, el médico también tendrá en cuenta la fase o la clasificación de la leucemia, la progresión de la enfermedad (cuánto se ha extendido), los factores pronósticos (características especiales que pueden influir en el curso de la enfermedad) y las estadísticas de supervivencia para el tipo particular de leucemia o trastorno.
Factores de riesgo para la leucemia
No hay una causa conocida ni única para la leucemia. La mayoría de los cánceres son el resultado de muchos factores de riesgo a la vez. Sin embargo, algunas personas con leucemia no tienen factores de riesgo identificables.
Los diferentes tipos de leucemia tienen diferentes factores de riesgo. Un factor de riesgo no puede aumentar el riesgo para todos los tipos de leucemia. No todos los factores de riesgo de los diferentes tipos de leucemia se enumeran a continuación.
Los hombres son más propensos que las mujeres a desarrollar leucemia. El riesgo para el desarrollo de la mayoría de los tipos de leucemia aumenta con la edad.
Los siguientes factores son conocidos por aumentar el riesgo de desarrollar algunos tipos de leucemia:
- altas dosis de radiación (como la exposición a explosiones de bombas atómicas o accidentes nucleares);
- radioterapia administrada en el pasado para tratar el cáncer u otros trastornos de salud;
- quimioterapia administrada en el pasado para tratar el cáncer;
- radioterapia combinada con quimioterapia administrada en el pasado (la combinación de los tratamientos aumenta el riesgo más que los tratamientos individuales);
- la exposición al benceno o formaldehído;
- síndromes genéticos (la leucemia se puede desarrollar en los niños con estos síndromes): síndrome de Down, anemia de Fanconi, ataxia-telangiectasia y síndrome de Bloom.
Tener sobrepeso u obesidad es un factor de riesgo para la leucemia. Esto significa que tiene una asociación con la leucemia, pero no hay suficiente evidencia para decir que es un riesgo conocido.
Los siguientes son factores desconocidos para los que no hay suficiente evidencia o la evidencia no es concluyente. En otras palabras, no se puede determinar con certeza si estos factores están o no asociados con la leucemia:
- las exposiciones a productos agrícolas y afines (en especial a los herbicidas o pesticidas);
- la exposición laboral a ciertos productos químicos o radiación en dosis bajas;
- la exposición a campos electromagnéticos.
No hay maneras específicas para reducir el riesgo de leucemia. Es importante que cualquier persona que tenga síntomas consulte a su médico tan pronto como sea posible. En especial vaya al médico si tiene los siguientes síntomas: fatiga, malestar, pérdida de apetito, pérdida de peso, sangrado o moretones, e infecciones frecuentes.
Diagnóstico y pruebas de la leucemia
Los exámenes de diagnóstico para la leucemia se realizan cuando: los síntomas de la leucemia están presentes, el médico sospecha que puede tener leucemia después de hablar con la persona y completar un examen físico, y cuando las pruebas de rutina de laboratorio sugieren un problema con la sangre.
Algunas de las pruebas que se usan para diagnosticar la leucemia inicialmente se utilizan también para determinar la etapa en la que está (cuánto ha avanzado).
Historia clínica y examen físico
La historia clínica es un registro de los síntomas actuales, factores de riesgo y todos los eventos médicos y problemas que una persona haya tenido en el pasado. El historial médico de la familia de una persona también puede ayudar al médico a diagnosticar la leucemia.
En la historia médica, el médico le hará preguntas sobre: historia personal de exposición a altas dosis de radiación, síndromes genéticos, exposición al benceno, quimioterapia o radioterapia previa, infecciones virales, historia familiar de leucemia, y signos y síntomas.
Un examen físico permite al médico detectar cualquier signo de leucemia. Durante un examen físico, el médico puede:
- medir los signos vitales para detectar fiebre, falta de aire y palpitaciones;
- evaluar la piel para ver si hay moretones y palidez;
- palpar las áreas del cuello, las axilas y la ingle para detectar los ganglios linfáticos inflamados o agrandados;
- examinar la boca en busca de infección y sangrado, o inflamación de las encías;
- palpar el abdomen en busca de órganos inflamados;
- examinar el esqueleto para detectar sensibilidad o dolor.
Análisis sanguíneo completo
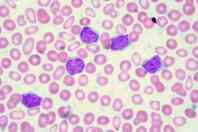
Un análisis sanguíneo completo mide la cantidad y calidad de los glóbulos blancos, glóbulos rojos y plaquetas. Se sospecha que hay leucemia cuando los recuentos de células sanguíneas son anormales y las células de la sangre no se ven normales. Los recuentos de células de sangre anormales pueden deberse a leucemia u a otros trastornos. Los glóbulos blancos inmaduros normalmente no se ven en la sangre, por lo que se sospecha de leucemia si están presentes.
- Leucemia aguda: El recuento de glóbulos blancos puede ser bajo, normal o alto. Las células blásticas pueden estar presentes en la sangre de personas con leucemia aguda. Muchas personas con leucemia aguda tienen neutropenia (neutrófilos bajos). Alrededor del 40% de las personas con leucemia aguda tienen trombocitopenia (recuento bajo de plaquetas). La mayoría de las personas con leucemia aguda tienen anemia (bajo número de glóbulos rojos).
- Leucemia crónica: El conteo de glóbulos blancos es elevado. El recuento de plaquetas puede ser bajo. Puede existir anemia.
Pruebas de química sanguínea
Las pruebas de química sanguínea miden ciertas sustancias químicas en la sangre que muestran si ciertos órganos están funcionando bien, y también se pueden usar para detectar anormalidades. Ayudan a detectar problemas del hígado o de los riñones causados por la propagación de las células leucémicas. Los siguientes niveles en sangre pueden estar elevados: nitrógeno de urea en sangre (BUN), creatinina, fosfato, lactato deshidrogenasa (LDH), transaminasas como la alanina aminotransferasa (ALT) y la aspartato transaminasa (AST), y
ácido úrico.
Factores de sangrado y coagulación
Las pruebas miden los factores de coagulación de la sangre para ver cómo el cuerpo puede coagular la sangre. En la leucemia pueden darse niveles anormales de factores de coagulación de la sangre. Se miden utilizando las siguientes pruebas: nivel de fibrinógeno, tiempo de protrombina (TP) o ratio internacional normalizado (INR), y tiempo de tromboplastina parcial (PTT).
Citoquímica
La citoquímica utiliza colorantes para identificar las estructuras de tejidos y componentes celulares en la sangre o en las células de la médula ósea. Algunos tintes son atraídos por ciertas sustancias que se encuentran en algunos tipos de células leucémicas. Los resultados de la tinción se pueden ver con un microscopio. La citoquímica ayuda a determinar el tipo de células que están presentes.
Citometría de flujo
La citometría de flujo es una prueba de laboratorio que se utiliza para clasificar, contar y examinar partículas microscópicas (como células o ADN). Las células se miden por tinción con un colorante sensible a la luz; se colocan en un fluido y pasan a través de un rayo láser. El láser hace que estas células emitan una luz que es medida y analizada por una computadora. La citometría de flujo ayuda a determinar los tipos de células que están presentes.
Inmunohistoquímica
Al igual que la citometría de flujo, la inmunohistoquímica (o inmunocitoquímica) trata una muestra de células de la sangre o de la médula ósea con anticuerpos especiales. En lugar de utilizar un láser y una computadora, se agregan sustancias químicas que hacen que la celda cambie de color si un determinado anticuerpo se adhiere a ella. El cambio de color sólo se puede ver con un microscopio. La inmunohistoquímica ayuda a determinar los tipos de células que están presentes.
Citogenética
Las técnicas citogenéticas en una muestra de sangre o de médula ósea sirven para ayudar a identificar los segmentos de cromosomas individuales y distinguirlos. Estas técnicas citogenéticas muestran anomalías cromosómicas que ayudan a confirmar el diagnóstico e identificar el tipo de leucemia. Los resultados también son útiles para planificar el tratamiento y predecir la respuesta al tratamiento. Los resultados para la prueba citogenética están generalmente disponibles dentro de 3-4 semanas.
Los cambios cromosómicos que ocurren en algunas personas con leucemia incluyen: translocaciones (parte de un cromosoma se adhiere a parte de un cromosoma diferente),
inversiones (parte de un cromosoma se desprende, voltea de extremo a extremo y entra en el mismo cromosoma), y pérdida o ganancia de cromosomas.
Hibridación fluorescente in situ (FISH)
La hibridación fluorescente in situ es similar a la prueba citogenética y se puede usar para detectar cambios específicos en los cromosomas de la sangre o las células de la médula ósea. Algunas anomalías que son demasiado pequeñas para ser encontradas con la prueba citogenética normal se pueden encontrar mediante esta técnica que usa tintes especiales que se adhieren sólo a partes específicas de determinados cromosomas. Es una técnica muy precisa y los resultados suelen estar listos en un par de días.
Reacción en cadena de la polimerasa (PCR)
La reacción en cadena de la polimerasa en (PCR) y la reacción en cadena de la polimerasa y la transcriptasa inversa (RT-PCR) son pruebas genéticas sensibles utilizadas para encontrar anormalidades específicas en la sangre o las células de la médula ósea. Las anormalidades pueden ser encontradas incluso si hay muy pocas células de leucemia presentes en una muestra de tejido.
Aspiración de médula ósea y biopsia
Durante una aspiración de médula ósea se extraen células de la médula ósea (biopsia) para que puedan ser examinadas en el laboratorio. El informe de patología del laboratorio confirmará si la persona tiene leucemia y, en caso afirmativo, qué tipo de leucemia.
Punción lumbar
Una punción lumbar extrae una pequeña cantidad de líquido cefalorraquídeo del espacio alrededor de la columna vertebral, para examinarla con un microscopio. El líquido cefalorraquídeo rodea el cerebro y la médula espinal. Una punción lumbar se realiza para ver si el cáncer se ha propagado al líquido cefalorraquídeo.
Biopsia de ganglios linfáticos
Se realiza una biopsia por escisión, en la que el ganglio linfático se elimina por completo y se examina bajo un microscopio para identificar el tipo de células y el patrón en el que están creciendo.
Radiografía del tórax
La radiografía de tórax se utiliza para buscar adenopatías mediastínicas (ganglios linfáticos en el centro del pecho), timo agrandado, acumulación de líquido alrededor de los pulmones y neumonía (infección pulmonar).
Tomografía computarizada
Una tomografía computarizada usa un equipo especial de rayos X para crear imágenes en tres dimensiones y una sección transversal de órganos, tejidos, huesos y vasos sanguíneos en el interior del cuerpo. Una computadora convierte las imágenes en imágenes detalladas. Se puede utilizar para mostrar los ganglios linfáticos agrandados alrededor del corazón, cerca de la tráquea o en la parte posterior del abdomen.
Resonancia magnética
La resonancia magnética utiliza fuerzas magnéticas potentes y ondas de radiofrecuencia para crear imágenes transversales de los órganos, tejidos, huesos y vasos sanguíneos. Una computadora convierte las imágenes en imágenes de tres dimensiones. Es útil para examinar el cerebro y la médula espinal. Se utiliza con mayor frecuencia cuando existe la preocupación de que la leucemia se haya diseminado al cerebro.
Ultrasonidos
El ultrasonido utiliza ondas sonoras de alta frecuencia para crear imágenes de estructuras internas del cuerpo. Se utiliza para ver si los órganos internos, como los riñones, el hígado o el bazo, se han visto afectados por la leucemia.
TRATAMIENTO DE LA LEUCEMIA
El tratamiento para la leucemia lo determinan los especialistas en cáncer (oncólogos), que a veces son especialistas en cirugía, en radioterapia y en quimioterapia (fármacos).
Las decisiones de tratamiento para la leucemia se basan en el tipo de leucemia, la edad de la persona, las anomalías cromosómicas (genéticas) y la salud general de la persona.
Las opciones de tratamiento para la leucemia son:
- quimioterapia: tratamiento principal para muchos tipos de leucemia;
- trasplante de células madre: una opción para algunas personas menores de 55 años;
- radioterapia: a menudo se utiliza para tratar o prevenir la propagación hacia el sistema nervioso central y para prepararse para el trasplante de células madre;
- terapia dirigida a quienes tienen el cromosoma Filadelfia (Ph);
- terapia de apoyo para gestionar las complicaciones del tratamiento;
- seguimiento después de finalizar el tratamiento.
Leucemia linfocítica aguda
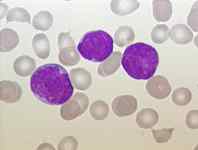 |
Las decisiones de tratamiento se basan en la edad, las anomalías cromosómicas, el subtipo de leucemia linfocítica aguda, la fase del cáncer, la salud general de la persona y la respuesta al tratamiento.
Una remisión completa (respuesta completa) significa que:
- Los recuentos de células de sangre periférica vuelven a los niveles normales.
- Menos del 5% de las células de la médula ósea son blastos.
Se considera enfermedad residual mínima cuando:
- Las pruebas estándar, como la observación de las células bajo un microscopio, no pueden encontrar células leucémicas en la médula ósea.
- Las pruebas más sensibles, como la citometría de flujo o la reacción en cadena de la polimerasa, encuentran evidencia de que todavía hay células leucémicas en la médula ósea.
Se considera enfermedad activa cuando la leucemia aún está presente durante el tratamiento o ha recidivado después del tratamiento.
La recaída significa que más del 5% de las células en la médula ósea son blastos.
Quimioterapia
La quimioterapia se utiliza durante todas las fases y para la profilaxis y el tratamiento del sistema nervioso central. Los medicamentos utilizados para tratar la leucemia linfocítica aguda incluyen: vincristina (Oncovin), daunorubicina (Cerubidine), doxorrubicina (Adriamicina), idarrubicina (Idamycin), mitoxantrona (Novantrone), citarabina (Cytosar, Ara-C), asparaginasa (Kidrolase), etopósido (VePesid, VP-16), teniposide (Vumon, VM-26), mercaptopurina (Purinethol, 6-MP), metotrexato (Metotrexato), ciclofosfamida (Cytoxan, Procytox), y esteroides como la prednisona (Deltasone) o dexametasona (Decadron, Dexasone).
Radioterapia
La radioterapia se utiliza para:
- prevenir o tratar la propagación de la leucemia linfocítica aguda a través del sistema nervioso central;
- la irradiación corporal total antes de un trasplante de células madre;
- para aliviar el dolor en los huesos;
- para tratar la propagación de la leucemia a áreas como los testículos o la piel;
- a veces se utiliza para reducir el tamaño del tumor, si está presionando la tráquea.
Trasplante de células madre
Esta terapia puede ser considerada para personas con leucemia linfocítica aguda en los siguientes casos:
- al principio de la primera remisión o después de una recaída si se puede lograr una remisión parcial o completa;
- se puede dar una infusión de linfocitos del donante para estimular el sistema inmune después de un trasplante de células madre.
Terapia dirigida
A las personas que tienen el cromosoma Filadelfia (Ph+) se les puede administrar imatinib (Gleevec) u otro inhibidor de la tirosina quinasa, como parte del régimen de quimioterapia.
Terapia de apoyo para atender las complicaciones del tratamiento
- Antibióticos y antifúngicos: medicamentos para combatir las infecciones.
- Productos sanguíneos. Terapia de reemplazo cuando el recuento de células sanguíneas es bajo.
- Factores de crecimiento: para estimular la producción de glóbulos blancos.
- Medicamentos para reducir los altos niveles de algunos productos químicos en la sangre que resultan de la muerte celular rápida en el comienzo del tratamiento.
- Leucaféresis: para eliminar un gran número de células blancas de la sangre.
Después de finalizar el tratamiento es importante contar con visitas de seguimiento frecuentes, sobre todo en los primeros 5 años después del tratamiento, incluso si no hay signos de enfermedad. El tiempo entre los exámenes será más largo conforme pasa el tiempo, pero continuará indefinidamente.
Leucemia mieloide aguda
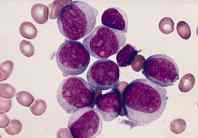 |
Los medicamentos de quimioterapia utilizados para tratar la leucemia mieloide aguda incluyen: citarabina (Cytosar, Ara-C), daunorubicina (Cerubidine), doxorrubicina (Adriamicina), idarrubicina (Idamycin), mitoxantrona (Novantrone), tioguanina (Lanvis, 6-TG), mercaptopurina (Purinethol, 6-MP), fludarabina (Fludara), etopósido (VePesid, VP-16), ciclofosfamida (Cytoxan, Procytox), topotecan (Hycamtin), metotrexato (Metotrexato), hidroxiurea (Hydrea), amsacrina (AMSA PD) y azacitidina (Vidaza).
Los medicamentos utilizados para tratar la leucemia promielocítica aguda incluyen: tretinoína (ácido trans-retinoico, ATRA, Vesanoid) y trióxido de arsénico.
Al igual que con la leucemia linfocítica aguda, se puede aplicar también radioterapia, transplante de células madre y terapia de apoyo.
Leucemia linfocítica crónica
 |
La quimioterapia puede administrarse como tratamiento primario para devolver los recuentos de células sanguíneas a la normalidad, para reducir el agrandamiento del bazo y para la leucemia linfocítica crónica recidivante o resistente al tratamiento.
Los medicamentos de quimioterapia usados incluyen: fludarabina (Fludara), cladribina (2-CDA, Leustatin), clorambucil (Leukeran), ciclofosfamida (Cytoxan, Procytox), vincristina (Oncovin) y doxorrubicina (Adriamicina). Un esteroide como la prednisona (Deltasone) puede administrarse en combinación con la quimioterapia.
La terapia biológica se aplicará en los siguientes casos: en leucemias linfocíticas crónicas de riesgo intermedio o alto, cuando ya no responde a la quimioterapia, y junto con la quimioterapia como tratamiento de primera línea o como terapia de segunda línea.
Las terapias biológicas utilizadas para tratar la leucemia linfocítica crónica son el alemtuzumab (Campath) y el rituximab (Rituxan).
Se puede hacer una esplenectomía (extirpación del bazo) si el bazo se agranda y las otras terapias no disminuyen el tamaño del bazo, y para ayudar a mejorar los recuentos de células sanguíneas.
La radioterapia puede aplicarse para reducir el tamaño del bazo si la quimioterapia no funciona, para aliviar el dolor óseo provocado por el crecimiento de células de leucemia en la médula ósea y para reducir el tamaño de los ganglios linfáticos en un área del cuerpo.
Actualmente no se usa trasplante de células madre para personas con leucemia linfocítica crónica, pero los investigadores continúan evaluando esta opción.
La terapia de apoyo para gestionar las complicaciones del tratamiento consiste en antibióticos y antifúngicos, gamma globulina (para ayudar a corregir la inmunodeficiencia), derivados sanguíneos, factores de crecimiento (para estimular la producción de glóbulos blancos), medicamentos para reducir los altos niveles de algunos productos químicos en la sangre debido a la muerte celular rápida en el comienzo del tratamiento, leucaféresis y corticosteroides.
Leucemia mielógena crónica
 |
Vigilancia de la enfermedad
La monitorización de la enfermedad durante el tratamiento se adapta a cada persona y puede ser similar al siguiente:
- recuento sanguíneo completo todas las semanas hasta que los recuentos sean estables, y luego mensualmente;
- pruebas citogenéticas (análisis de las células) de la médula ósea al momento del diagnóstico, a los 6 y 12 meses después de comenzar el tratamiento, y luego cada año con tratamiento continuo;
- prueba de PCR o PCR transcriptasa inversa (RT-PCR) en sangre al momento del diagnóstico y aproximadamente cada 3 meses con tratamiento continuo.
Respuesta hematológica
La respuesta hematológica generalmente se presenta dentro de los primeros 3 meses de iniciar el tratamiento, y puede ser:
- Respuesta hematológica completa. Los recuentos de células sanguíneas han vuelto a la normalidad, no hay células inmaduras en la sangre y el bazo ha vuelto a su tamaño normal.
- Respuesta hematológica parcial. Es similar a una respuesta completa pero no se dan las tres condiciones anteriores.
Respuesta citogenética
La respuesta citogenética puede tardar varios meses o más en producirse. Una respuesta citogenética parcial dentro de 3-6 meses de iniciado el tratamiento predice una probabilidad del 80-95% de lograr una respuesta citogenética completa. De igual forma que la anterior, pueden darse varios tipos de respuesta:
- Respuesta citogenética completa. No hay células con el cromosoma Filadelfia en la sangre o la médula ósea.
- Respuesta citogenética parcial. Menos del 35% de las células tienen el cromosoma Filadelfia.
- Respuesta citogenética mayor. Se utiliza a veces para hacer referencia a una respuesta completa o parcial.
- Respuesta citogenética menor. Un 35-90% de las células tienen el cromosoma Filadelfia.
No hay un plazo específico para una respuesta citogenética completa antes de que los médicos consideren un tratamiento diferente. Un enfoque de tratamiento diferente se decide sobre una base individual, según la edad de la persona y otras opciones de tratamiento posibles.
Respuesta molecular
La respuesta molecular se basa en los resultados de la prueba de reacción en cadena de la polimerasa (PCR). Puede ser de dos tipos:
- Respuesta molecular completa. El gen BCR-ABL no se encuentra en la sangre.
- Respuesta molecular mayor. Una cantidad muy baja de gen BCR-ABL se encuentra en la sangre.
La terapia dirigida con inhibidores de la tirosina kinasa son el tratamiento de primera línea para la mayoría de las personas con leucemia mielógena crónica. Los inhibidores empleados incluyen imatinib (Gleevec), dasatinib (Sprycel) y nilotinib (Tasigna).
El trasplante de células madre es la terapia de primera línea para algunas personas durante la fase crónica de la enfermedad y la terapia de segunda línea después de que la leucemia se vuelve resistente al tratamiento con imatinib, dasatinib o interferón alfa. Un trasplante de intensidad reducida puede ser una opción para las personas mayores. Una infusión con linfocitos del donante se puede dar para estimular el sistema inmunológico cuando hay una recaída después de un trasplante de células madre.
La terapia biológica con interferón alfa (Intron A, Roferon A) solía ser el tratamiento de primera línea para la leucemia mielógena crónica. Todavía se utiliza para tratar a personas que no pueden tolerar otras terapias o cuya leucemia es resistente a la terapia dirigida.
La quimioterapia fue hace un tiempo uno de los principales tratamientos para la leucemia miélogena crónica. Todavía se utiliza para tratar a las personas cuando la terapia dirigida ha dejado de funcionar, y es parte del tratamiento durante un trasplante de células madre.
Los medicamentos de quimioterapia usados incluyen: busulfán (Myleran [oral] Busulfex [intravenosa]), hidroxiurea (Hydrea, Apo-hidroxiurea, Gen-hidroxiurea) y citarabina (Cytosar, Ara-C).
Una esplenectomía (extirpación quirúrgica del bazo ) se puede realizar si el bazo se agranda y es doloroso, y también cuando la quimioterapia o la radioterapia no ayudan a hacer el bazo más pequeño. El bazo también se puede quitar para ayudar a mejorar los recuentos de células sanguíneas.
Como en el caso de otros subtipos de leucemia, también puede emplearse radioterapia y terapia de apoyo.
Anatomía y fisiología de la sangre
La sangre está compuesta de líquido (llamado plasma) y células sólidas. La médula ósea es la sustancia suave y esponjosa en el centro de los huesos donde se producen las células sanguíneas.
Estructura de la sangre
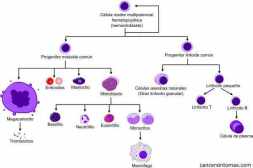 |
Todas nuestras células sanguíneas se desarrollan a partir de células madre. El proceso de desarrollo de células sanguíneas se denomina hematopoyesis. En las primeras etapas de desarrollo de las células sanguíneas, las células madre comienzan a convertirse a lo largo de la línea celular linfoide o mieloide. En ambas líneas celulares, las células madre se convierten en blastos, que todavía son células inmaduras. Durante la última etapa del desarrollo de las células, los blastos maduran en tres tipos de células de la sangre llamadas glóbulos rojos, plaquetas y glóbulos blancos.
Función de la sangre
La función principal de la sangre es suministrar nutrientes, eliminar los desechos de las células, transportar hormonas a los tejidos y proteger el cuerpo contra microorganismos dañinos. Cada tipo de célula sanguínea tiene un trabajo específico. Los glóbulos rojos transportan oxígeno desde los pulmones al resto del cuerpo y devuelven el dióxido de carbono a los pulmones. Las plaquetas forman coágulos de sangre en los vasos dañados para detener el sangrado. Los glóbulos blancos (leucocitos) ayudan a prevenir y combatir la infección por bacterias y virus, y destruyen otras células o sustancias extrañas.
Tipos de células blancas de la sangre
Las células blancas de la sangre se clasifican en linfocitos, granulocitos y monocitos.
- Linfocitos (de la línea de células linfoides). Los linfocitos producen anticuerpos para combatir las infecciones. Se encuentran en los ganglios linfáticos, el timo, el bazo, las amígdalas, la adenoides, la médula ósea y en el tejido linfático en otras partes del cuerpo como el estómago y el revestimiento intestinal. Hay de varios tipos: células B (que producen anticuerpos para combatir las bacterias, virus y hongos), células T (que activan las células B para producir anticuerpos) y células asesinas naturales (NK) (que atacan a las células extrañas).
- Granulocitos (desde la línea de células mieloides). Los granulocitos destruyen las bacterias para combatir infecciones. Hay tres tipos: neutrófilos (que son las principales células que combaten la infección, ingiriendo o fagocitando las células extrañas), eosinófilos (que ayudan a controlar la inflamación y las reacciones alérgicas, y atacan y destruyen ciertos organismos parasitarios), y basófilos (que juegan un papel en ciertas reacciones alérgicas).
- Monocitos (desde la línea de células mieloides). Los monocitos ayudan a combatir la infección por la ingestión de sustancias como las bacterias y los hongos.